Репродуктивное здоровье человека в системе радиационной безопасностиОпубликовано в журнале Медицинская радиология и радиационная безопасность (http://www.medradiol.ru). 2016. № 5 Введение Репродуктивная система – одна из важнейших систем организма, нарушения в которой приводят к серьёзным не только медицинским, но и социальным проблемам, поскольку генетические эффекты, возникающие при облучении гонад, потенциально способны затрагивать семью и общество в целом. Учитывая это, в международной системе радиационной безопасности защите гонад уделяется особое внимание. Материал и методы Анализировали семейное положение, возраст мужчин на момент рождения ребенка, показатели репродуктивной функции, такие как неблагоприятные исходы беременности у женщин (самопроизвольные аборты, мертворождения, ранняя неонатальная смертность новорожденных), задержка внутриутробного развития плода и ВПР
у детей, заболевания и осложнения беременностей у женщин с целью исключения
возможного влияния на развитие плода «материнского фактора», связанного с возрастом и состоянием здоровья женщины, условиями её труда (профессиональные вредности) и отмеченными вредными привычками (курение, алкоголь). Результаты и обсуждение
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Группа | Карты беременных (ф. 32) |
История развития ребёнка (ф. 112/у) и амбулаторные карты (ф. 025/у) |
| Персонал АЭС – участники ЛПА | 420 | 332 |
| Персонал АЭС, не участвовавший в ЛПА | 470 | 547 |
| Городское население | 508 | 587 |
| ВСЕГО | 2864 | |
В табл. 2 представлены данные о неблагоприятных последствиях для детей различных условий облучения отца. Приведенные данные свидетельствуют, что в семьях мужчин группы персонала участников ЛПА достоверно выше летальные детские потери, в основном, за счёт самопроизвольных абортов. Общая частота этих потерь у персонала участников ЛПА составила 187±21, а в группе персонала, не работавшего по ЛПА – 93,2±13,4 на 1000 беременных женщин. У детей персонала участников ЛПА достоверно выше, чем у детей персонала, частота ВПР – 111±17 и 82,3±11,8 на 1000 соотв., и выше общая задержка развития плода (ЗВУР) – 175±17 и 83,7± 11,4 на 1000 соотв., которая, согласно Публикации 103 МКРЗ, может рассматриваться, наряду с ВПР, в качестве возможного наследственного эффекта.
Таблица 2
Сравнительная характеристика неблагоприятных последствий для детей различных условий облучения отца
| Показатель | Группа | ||
| Городское население | Персонал АЭС, не участвовавший в ЛПА | Персонал АЭС – участники ЛПА | |
| Оцененные дозы облучения до зачатия, мЗв | – | От 12 до 70 | От 70 до 130 |
| Общая заболеваемость детей, на 1 000 | 3310±194 | 3623±206 | 5184±267* |
| Частота ВПр, на 1 000 новорожденных | 52,5±12,4 | 82,3±11,8 | 111±17* |
| Заболеваемость ЗВУр, на 1 000 новорожденных | 77,4±14,8 | 83,7±11,4 | 175±17* |
| Летальные потери, на 1 000 беременных, в т.ч.: | 73,8±8,4 | 93,2±13,4 | 187±21* |
| самопроизвольные аборты | 56,7±12,8 | 72,3±11,1 | 163±14* |
| мертворождения | 5,3±2,3 | 8,6±4,3 | 9,2±6,9 |
| ранняя неонатальная смертность | 11,8±3,5 | 12,3±5,1 | 15,3±4,9 |
Примечание: * – в сравнении с группой персонала АЭС различия достоверны (p < 0,05)
Отраслевой регистр лиц, подвергшихся воздействию радиации в результате аварии на Чернобыльской
АЭС, являясь самым крупным из отраслевых регистров соответствующего профиля, содержит данные только на 9,3% от общего числа ликвидаторов аварии на
ЧАЭС, зарегистрированных в Национальном радиационно‑эпидемиологическом регистре (НРЭР). По данным отраслевого регистра у участников
ЛПА в период 1987–1992 гг. были реализованы 85% всех случаев деторождений. Затем число деторождений прогрессивно сократилось. В целом по отраслевому регистру
ФМБА частота ВПР у детей участников ЛПА составляет 134 на 1 000 новорожденных [4]. Согласно Национальному регистру, частота ВПР у детей – около 130–160 случаев на 1000 новорожденных для ликвидаторов‑мужчин в возрасте 25–30 лет. Зависимость частоты ВПр от зарегистрированных доз облучения не установлена. Общая численность группы ликвидаторов‑мужчин в НРЭР – 188 701 чел., и их детей – 21 395 чел. [5].
Выявленные изменения в показателях репродуктивного здоровья мужчин персонала участников
ЛПА, получивших суммарные дозы облучения 70–130 мЗв, сопоставимы с изменениями показателей здоровья у ликвидато‑ ров, не являющихся персоналом
АЭС, получивших дозы облучения 50–250 мЗв (в среднем 118 мЗв).
Вместе с тем, в соответствии с положением НРБ‑99/2009 «лица,
подвергшиеся облучению в эффективной дозе, превышающей 100 мЗв в течение года, при дальнейшей работе не должны подвергаться облучению в дозе свыше 20 мЗв за год», то есть к моменту зачатия через 5–6 лет после аварийного облучения в дозах до 200 мЗв, разрешается получать еще 100–120 мЗв. таким образом, допускается суммарная доза до зачатия свыше 300 мЗв.
Приведенные фактические и опубликованные данные [4, 6–10]
показывают, что негативные изменения у потомства возникают при облучении мужчин в дозах в среднем 100 мЗв и выше. Следовательно, облучение в дозах 200–300 мЗв нельзя считать безопасным, а существующую систему ограничений планируемого повышенного аварийного облучения считать достаточно эффективной.
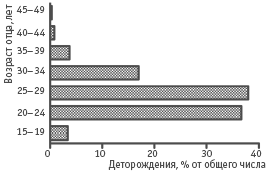 Рис. 1. распределение общего числа деторождений по возрастным группам мужчин – персонала САЭС |
Число деторождений само по себе не является показателем репродуктивного здоровья мужчины, поскольку во многом зависит от социально‑экономических
условий жизни и осознанного выбора человека и семьи. Таким же условным является и верхний предел репродуктивного возраста мужчин. С точки зрения радиологической защиты важно знать возраст мужчины для оценки ожидаемого генетического риска для всех детей, а не только родившихся у мужчин в возрасте до 30 лет. В соответствии с
НРБ‑99/2009 для условий работы с плановым повышенным облучением, защищаемый репродуктивный возраст мужчин продолжается с 18 до 30 лет, и, следовательно, дети, рожденные у мужчин в возрасте старше 30 лет, могут составлять группу риска.
Изучения семейного положения персонала САЭС показало, что деторождения в возрасте мужчины старше 30 лет отмечены у 27,1% мужчин (рис. 1).
Фактические дозы облучения мужчин к моменту зачатия ребенка составили 51,0 мЗв, в том числе, к моменту рождения первого ребенка – 42,7 мЗв, второго ребенка – 64,4 мЗв и третьего ребенка – 96,2 мЗв (табл. 3).
Таблица 3
Распределение деторождений в семьях мужчин персонала САЭС по дозовым группам
| Показатель | Деторождения | |||
| 1‑е | 2‑е | 3‑е | 4‑е | |
| Средняя доза, мЗв | 42,7 | 64,4 | 96,2 | 56,0 |
| Диапазон доз, мЗв | 5–125 | 10–300 | 30–258 | – |
| Удельный вес лиц с дозой свыше 100 мЗв, % | 2 | 5 | 15 | – |
Таблица 4
Шкала оценки риска [11]
| Оценка риска | Значение коэффициента относительного риска, Кр |
| Минимальный риск | 0–0,1 |
| Допустимый риск | 0,1–0,3 |
| Высокий риск | 0,3–0,6 (0,7) |
| Недопустимый риск | более 0,6 (0,7) |
Распределение деторождений у мужчин приходится, в основном, на возрастной диапазон от 20 до 35 лет и одинаково в сравниваемых группах.
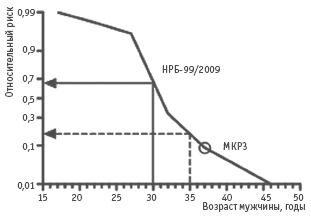 Рис. 2. Вероятность выявления наследственных эффектов у потомков мужчин – персонала АЭС |
Используя распределение возрастных коэффициентов рождаемости и предлагаемую шкалу оценки риска (табл. 4), была рассмотрена вероятность выявления
(на основе ожидаемого числа деторождений) генетических эффектов у
потомства мужчин разного возраста (рис. 2). Представленная
зависимость показывает, что НРБ‑99/2009 реализуют «защиту» репродуктивного здоровья (до 30 лет) на уровне границы между риском высоким и риском недопустимым, тогда как
МКРЗ рекомендует «удерживать» риск генетических последствий в области минимального [11].
Снижение риска негативных последствий облучения мужчин (мутаций у потомства) не может быть достигнуто только ужесточением предельных доз облучения. Снижение доз аварийного и последующего профессионального облучения
хотя и снижает риск возможных генетических эффектов у потомства, но
не исключает его в должной мере. В этой связи разумным подходом представляется увеличение срока продолжительности защищаемого репродуктивного периода у мужчин, на который распространяются ограничения профессионального и аварийного облучения, с граничного 30‑летнего возраста, как это принято сейчас, до возраста в 35 лет. Этот подход, обеспечивающий защиту до 95% потомков первого поколения облученных отцов, позволит рассматривать ситуации планового повышенного и аварийного облучения персонала, как имеющие достаточный и «разумно достижимый уровень» защиты от вероятных неблагоприятных генетических эффектов облучения.
При этом следует отметить, что возраст мужчины 35 лет в большей степени отвечает положению
МКРЗ, которая определяет длительность защищаемого репродуктивного периода, как 1/3 от 50 лет профессиональной
деятельности, которая продолжается с 20 до 70 лет (то есть до возраста 36–37 лет) [12].
Профессиональное облучение в штатных условиях
Целью данного раздела работы явилась оценка возможного генетического риска облучения мужчин персонала САЭС и
КАЭС, работающих в штатных условиях профессионального облучения. И хотя принятые в настоящее время в качестве пределов дозы профессионального облучения уровни в 20 мЗв/год, в среднем за любые последовательные 5 лет, но не более 50 мЗв/год, исключают появление детерминированных эффектов, но не исключают при этом некоторый генетический риск.
Исследовали состояние репродуктивного здоровья в соответствии с методикой, изложенной выше. В качестве показателей возможных генетических эффектов анализировали частоту ВПР и перинатальных потерь, 80% которых обусловлены врожденными пороками.
Средние дозы профессионального облучения мужчин, работающих на
АЭС, полученные к моменту зачатия детей и за весь репродуктивный период, и
являющиеся основой для оценки возможных генетических эффектов у потомства, представлены в табл 5.
Таблица 5
Дозы профессионального облучения мужчин, работающих на АЭС, мЗв
| Показатель | 1987–1992 г г. | 2001–2012 г г. |
| Средняя годовая доза | 12,5 | 2,2 |
| Диапазон доз к моменту зачатия | 12,5–70,0 | 10,6–20,0 |
| Доза за весь репродуктивный период (10 лет) | 125,0 | 22,0 |
Уровень реальных средних годовых доз облучения работников
АЭС к периоду 2001–2012 гг. по сравнению с периодом 1987–1992 гг. снизился с 12,5 мЗв/год до 2,2 мЗв/год, т.е. более чем в 5 раз. Соответственно снижению среднегодовых доз облучения снизился и уровень доз, накопленных мужчинами за весь репродуктивный период жизни: 125 мЗв и 22 мЗв.
Результаты исследования частоты ВПР и перинатальных потерь (мертворождения и ранняя неонатальная
смерть новорожденных) в семьях персонала и мужчин, не работавших на АЭС (контрольная группа), в периоды 1987– 1992 гг. и 2001–2012 гг. представлены в табл. 6.
Таблица 6
Врожденные пороки развития и перинатальные потери в семьях мужчин персонала АЭС в разные периоды наблюдения, на 1000 новорожденных
| Показатель | 1987–1992 гг. | 2001–2012 г г. | ||
| персонал | контроль | персонал | контроль | |
| Всего новорожденных, абс. число | 547 | 587 | 1631 | 3183 |
| ВПР | 82,3±11,8 | 52,5±12,4 | 34,0±4,5 | 31,6±3,1 |
| Мертворождения | 8,6±4,3 | 5,3±2,3 | 5,8±1,5 | 6,4±2,8 |
| Ранняя неонатальная смертность | 12,3±5,1 | 11,8±3,5 | 1,6±1,1 | 2,8±1,4 |
| Всего НИБ | 103,2±12,8 | 69,6±10,1 | 41,4±4,9 | 40,8±3,5 |
Анализ приведенных данных показывает, что за время с 1987–1992 гг. к 2001–2012 гг. частота неблагоприятных исходов беременности (НИБ)
в семьях мужчин персонала АЭС снизилась более чем в 2,5 раза: с 103,2±12,8 до 41,4±4,9 на 1000 новорожденных. Основное снижение произошло за счёт снижения частоты ВПР – в 2,5 раза: с 82,3±11,8 до 34,0±4,5 на 1000 новорожденных, и ранней неонатальной смерти ребенка – в 7,5 раз: с 12,3±5,1 до 1,6±1,1 на 1000 новорожденных.
Следует отметить, что в 1987–1992 гг. частота ВПР у
новорожденных в семьях мужчин персонала статистически недостоверно превышала контрольные значения и уровень в 60 случаев на 1000 новорожденных, принятый
МКРЗ при оценке радиационно‑индуцированных пороков развития в качестве спонтанного. В период 2001–2012 гг. уровень ВПР
у новорожденных в семьях персонала не превышал контрольные значения и был значительно ниже спонтанного уровня
МКРЗ для оценки (расчета) радиационного риска.
Эти данные свидетельствуют, что переход на принцип нормирования с учетом стохастических эффектов и снижение среднегодовых доз профессионального облучения привело к значительному снижению риска наследственных эффектов у персонала, работающего в условиях воздействия ионизирующего излучения.
Выводы
- Установленные в отечественных НРБ‑99/2009 принципы и подходы к защите гонад лиц репродуктивного возраста в основном соответствуют принципам и подходам, принятым в международной системе радиационной защиты. Основой защиты справедливо принимаются принципы предотвращения детерминированных эффектов и снижения риска стохастических эффектов до разумно достижимого низкого уровня.
- Установленные в НРБ‑99/2009 требования ограничения аварийного и последующего профессионального облучения мужчин не обеспечивают в должной мере защиту детей от генетических последствий и требуют корректирования в направлении гармонизации с положениями, принятыми в международной системе радиационной защиты.
- Состояние здоровья детей мужчин персонала, подвергшихся плановому повышенному аварийному облучению и последующему профессиональному облучению в дозах от 70 до 130 мЗв, накопленных к моменту зачатия, характеризуется достоверным увеличением, по сравнению с аналогичными показателями в группе детей персонала, облучавшегося в дозах от 12 до 70 мЗв:
– общей заболеваемости: 5184±267 и 3623±206 на 1000 детей соответственно;
– частоты врождённых пороков развития: 111±17 и 82,3±11,8 на 1000 новорожденных соответственно;
– частоты задержки внутриутробного развития: 175±17 и 83,7±11,4 на 1000 новорожденных соответственно. - Принятый граничный репродуктивный возраст мужчин – 30 лет – и связанные с ним ограничения не обеспечивают защиту 25–30 % детей, рожденных после 30 лет.
- Увеличение срока продолжительности защищаемого репродуктивного периода у мужчин, на который распространяются ограничения профессионального и аварийного облучения до 35 лет, позволит исключить риск возможных генетических эффектов, обусловленных облучением их отцов, практически у 90–95 % потомства.
- Представляется спорным положение норм о необязательности запрета («как правило»), а также о «добровольном письменном согласии», так как оно фактически затрагивает интересы третьих лиц (семья, потомки) и общества в целом, которые никак не могут быть решены «согласием или несогласием» лица, подвергающегося риску, связанному с облучением, но не наделенного в этом случае никакими полномочиями для принятия подобного решения и никакой ответственностью по его исполнению.
Предложения по совершенствованию отдельных положений норм радиационной безопасности (НРБ‑99/2009)
С целью совершенствования требований ограничения аварийного и последующего профессионального облучения мужчин предлагается следующее:
- Продление мер защиты репродуктивного здоровья мужчин‑персонала группы а до граничного возраста не ниже 35 лет (в части планируемого аварийного облучения).
- Неприемлема и должна быть исключена формулировка необязательности («как правило») применения защитных мер для мужчин репродуктивного возраста. аргументы, которыми обосновывается необходимость привлечения к срочным противоаварийным мероприятиям лиц младшего возраста (чем установленный защищаемый возраст) могут рассматриваться только как возможное исключение, и только в условиях уже развивающейся аварии в изолированном окружении (атомная подводная лодка), но не могут приниматься во внимание при планировании противоаварийных мероприятий и служб для любых гипотетических аварийных ситуаций.
- Требует широкого обсуждения и прохождения этической экспертизы положение норм о «достаточности» для лиц репродуктивного возраста «добровольного письменного согласия», так как тут фактически затрагиваются интересы третьих лиц (семья, потомки) и общества в целом, которые никак не могут быть решены только лишь «согласием или несогласием» лица, подвергающегося риску, связанному с облучением. Добровольное согласие, как результат взвешенного решения информированного человека о «принятии» им потенциального «личного ущерба», теряет свой изначальный смысл, так как лицо, соглашающееся на потенциальный вред, казалось бы, собственному репродуктивному здоровью, фактически перекладывает вероятные проблемы на третьих лиц, посредством которых этот риск будет реализовываться.
СПИСОК ЛИТЕРАТУРЫ
- Рекомендации Международной комиссии по радиологической защите 1990 г. Публикация 60 МКРЗ. Часть 2. Под ред. И.Б. Кеирим‑Маркуса. – М. : Энергоатомиз‑ дат, 1994. 208 с.
- Нормы радиационной безопасности (НРБ‑99/2009). Санитарно‑эпидемиологические правила и нормативы. – М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора. 2009. 100 с.
- Публикация 103 Международной Комиссии по радиационной защите (МКРЗ). Пер. с англ. Под общей ред. М.Ф. Киселева и Н.К. Шандалы. – М.: Изд. ООО ПКФ «Алана». 2009. 312 с.
- Лягинская А.М., Туков А.Р., Осипов В.А. и соавт. Врожденные пороки развития у потомства ликвидаторов последствий аварии на Чернобыльской АЭС // Радиац. биология. Радиоэкология. 2009. 49. № 6. С. 694–702.
- Российский национальный доклад. 30 лет Чернобыльской аварии. Итоги и перспективы преодоления ее последствий в России 1986–2016. Под ред. В.А. Пучкова и Л.А. Большова. – М. 2016. 202 с.
- Sever L.E., Gilbert E.S., Hessol N.A., McIntyre J.M. A case‑control study of congenital malformations and occupational exposure to low‑level ionizing radiation // Amer. J. Epidemiol. 1988. Vol. 127. P. 226–242.
- Лягинская А.М., Головко О.В., Ермалицкий А.П., Купцов В.В. Реализация репродуктивной функции ликвидаторов последствий аварии на Чернобыльской АЭС, проживающих в Рязанской области // Вестн. рос. ассоц. акушеров‑гинекологов. 1996. №3. С. 84–87.
- Parker L., Pearce M.S., Dickinson H.O. et al. Stillbirths among ofspring of male radiation workers at Sellafeld nuclear reprocessing plant // Lancet. 1999. Vol. 354. № 9180. P. 1407–1414.
- Петрушкина Н.П. Здоровье потомков (1–2 поколение) работников первого предприятия атомной промышленности производственного объединения «Маяк» (клинико‑эпидемиологическое исследование). Дисc. докт. мед. наук. – М. 2003. 371 с.
- Dinshaw K.A., Notani P.N., Sachdev M.R. No Excess Cancer Risk to Radiation Workers. Condensed from the report entitled Efects of Low‑Dose Ionising Radiation among the Employees at the Tarapur DAE Centre: A Cross‑sectional Study prepared by Tata Memorial Centre. Mumbai. 2008. 8 pp.
- Ермалицкий А.П. Обеспечение эффективности радиационно‑гигиенических мер при защите репродуктивного здоровья мужчин, работающих в контакте с ионизирующими излучениями. Дисc. канд. мед. наук. – М. 2012. 119 с.
- Ермалицкий А.П., Лягинская А.М. Развитие современной системы защиты гонад и плода в международных рекомендациях (МКРЗ) и отечественных нормах радиационной безопасности // Мед. радиология и радиац. безопасность. – 2012, 57, № 4. – С. 5–12.